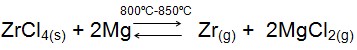O zircônio é um metal branco prateado em estado metálico quando purificado e cinza prateado em estado impuro, maleável e dúctil. Foi descoberto no ano 1789 por Klaproth, a partir do minério conhecido por zircão, ZnSiO4. Seu nome é proveniente do persa “zargum” que significa cor de ouro em virtude da coloração do minério citado. E foi posteriormente isolado por Berzélius em 1824. Possui número atômico 40, massa atômica relativa 91,22 u em função de ser o isótopo mais estável entre os 15 existentes, seu ponto de fusão é 1852ºC e ponto de ebulição 4377ºC, sua configuração eletrônica é 1s2 2s2 2p6 3s2 3p6 4s2 3d104p6 5s2 4d2. É um metal possuidor de propriedades semelhantes a do titânio, é um metal de transição pertencente à família IVB da tabela periódica e o seu símbolo químico é Zr.
Quimicamente o zircônio é um metal semelhante ao titânio apresentando propriedades de resistência a corrosão nas CNTP, não é atacado pela maioria dos ácidos, somente sendo atacado por ácido fluorídrico a qualquer concentração. A resistência do metal a corrosão se deve a camada de óxido inerte que é formada logo que este é exposto ao ar atmosférico, em forma de pó inflama-se em contato com o ar. É comumente encontrado na natureza na forma de silicato e óxido do metal. É obtido através do processo de Kroll, que consiste na conversão do minério em cloreto com posterior redução em presença de magnésio metálico.
Processo de Kroll:
O zircônio é um metal que apresenta uma reatividade relativamente baixa, na temperatura normal formando poucos compostos tais como nitretos, óxidos, silicatos e haletos, sendo estes seus compostos comumente conhecidos e mais utilizados.
Apesar de sua pouca reatividade química nas CNTP, o metal é amplamente utilizado industrialmente, seu maior uso está concentrado nas usinas nucleares, por que em virtude de sua baixa capacidade de absorção de nêutrons o metal é utilizado para revestir internamente os reatores nucleares evitando o desperdício de combustível nuclear, facilitando a movimentação dos nêutrons.
É utilizado também na fabricação de jóias, por que depois de polido, o zircônio assemelha-se a um diamante, além da resistência conferida pelo óxido formado, que é translúcido e inerte, é usado como material refratário na fabricação de cerâmicas e vidrarias laboratoriais e como catalisador em sínteses orgânicas. Além de ser utilizado na fabricação “flashes” fotográficos, forma ligas supercondutoras com nióbio em meio criogênico, o nitreto é empregado na fabricação de ferramentas em virtude da resistência mecânica conferida. Na área da saúde o zircônio é utilizado no implante de dentes e na fabricação de matérias-primas farmacêuticas. Segundo pesquisadores o zircônio é abundante fora da terra, visto que as análises de rochas lunares encontraram um alto teor do metal em sua composição química.
Atualmente existem estudos mostrando que uma liga de lítio e zircônio é capaz de absorver gás carbônico da atmosfera e armazenar afim de transportar para outro local, e reaproveitar a liga para um novo procedimento; resumindo isto significa a solução para uma parte dos problemas ambientais.
Na natureza não é encontrado em estado elementar, sendo encontrado somente na forma de minérios. Os mais comuns são o zircão ZrSiO4 (silicato de zircônio) e o baddeleyite ZrO2(óxido de zircônio) entre outros minérios. Os minérios de zircônio geralmente contêm também porções de Háfnio.
Bibliografia :
Mahan, B. M. Química: um curso universitário. 4a ed. São Paulo: Edgard Blücher, 2003.
SHRIVER, DUWARD; ATKINS, PETER. Química inorgânica - 4ª edição. Porto Alegre, Bookman, 2008.
LEE, J.D.. Química inorgânica não tão concisa – tradução da 4ª edição inglesa.São Paulo, Edgard Blücher, 1996.
Texto originalmente publicado em https://www.infoescola.com/elementos-quimicos/zirconio/