Para provar que os átomos não são maciços, como previa a Teoria de Dalton, Ernest Rutherford elaborou uma experiência, em 1911, onde ele bombardeou com partículas alfa (provenientes de uma amostra do elemento polônio, que é radioativo) uma fina placa de ouro.
Ele então notou que a maior parte dessas partículas atravessava a lâmina, e pouquíssimas eram repelidas ou desviadas.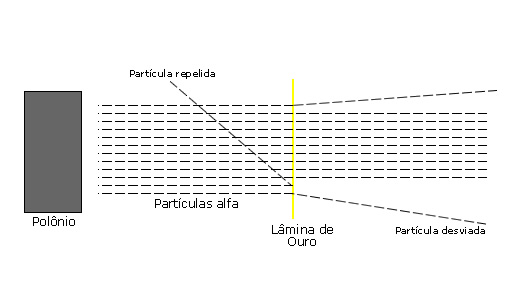 O motivo de algumas partículas serem repelidas é que bateram de frente com o núcleo atômico do ouro. As que sofreram desvio passaram muito perto do núcleo, pois a partícula alfa é de carga positiva, e o núcleo do ouro também.
O motivo de algumas partículas serem repelidas é que bateram de frente com o núcleo atômico do ouro. As que sofreram desvio passaram muito perto do núcleo, pois a partícula alfa é de carga positiva, e o núcleo do ouro também.
Assim, a Experiência de Rutherford provou que o átomo possui um grande vazio, um espaço muito grande entre os elétrons e os prótons do núcleo.
Leia mais:
Texto originalmente publicado em https://www.infoescola.com/quimica/experiencia-de-rutherford/