O frâncio é um metal alcalino (portanto, grupo 1 da tabela periódica) de número atômico Z = 87 e massa atômica ponderada igual a 223 (praticamente o único isótopo levado em consideração nesse cálculo é o Fr-223, pois é o mais estável. Com meia-vida igual a quase 22 minutos).
 É o segundo elemento mais raro da Terra (atrás apenas do astato), altamente radioativo e instável. Portanto, para reunir uma quantidade considerável deste metal, é necessário sintetizá-lo em laboratório.
É o segundo elemento mais raro da Terra (atrás apenas do astato), altamente radioativo e instável. Portanto, para reunir uma quantidade considerável deste metal, é necessário sintetizá-lo em laboratório.
Conteúdo deste artigo
Propriedades Físico-químicas
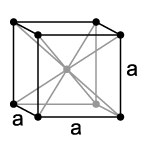 O retículo cristalino do frâncio apresenta estrutura do tipo cúbica de corpo centrado (ccc). E, o único estado de oxidação detectado em condições não-extremas é o +1 (comum a todos os alcalinos).
O retículo cristalino do frâncio apresenta estrutura do tipo cúbica de corpo centrado (ccc). E, o único estado de oxidação detectado em condições não-extremas é o +1 (comum a todos os alcalinos).
Possui o menor valor de eletronegatividade de todos os elementos da tabela (0,7, na escala Pauling) e, pelo menos em tese, formaria uma base forte (segundo teoria de Arrhenius) em meio aquoso.
A densidade do frâncio é relativamente baixa para um metal, 1870 Kg/m³, assim como os valores de ponto de fusão e ebulição: 27°C e 277°C, respectivamente. Ou seja, assim como o Gálio e o Césio, também sofreria fusão caso puséssemos na palma da mão.
A condução de calor no frâncio dá-se de forma 5 vezes menos intensa em relação à condução no ferro, mostrando, então, características de mau condutor. O mesmo não pode ser afirmado para a condução de eletricidade, pois os valores ainda são praticamente desconhecidos ou imprecisos.
Ocorrência e Aplicação
O frâncio é extremamente raro na crosta terrestre. Vagos vestígios são encontrados em minérios de urânio (pois faz parte da série de desintegrações deste).
Pode ser sintetizado através de uma reação envolvendo núcleos de ouro Au-197 e oxigênio O-18; deste processo, os isótopos Fr-209, Fr-210 e Fr-211 são gerados. Outro método de obtenção dá-se pelo bombardeio de tório com prótons; rádio ou astato com nêutrons.
De qualquer forma, a quantidade produzida até hoje não foi tão grande e, mesmo que fosse, acabaria de forma muito rápida (já que o frâncio decai, no máximo , a cada 22 minutos). Por isso, estudos mais profundos não foram realizados e as únicas aplicações existentes se encontram no campo de pesquisas científicas.
Ação biológica
Apesar de bastante escasso, apenas um pequeno montante de frâncio pode ser necessário para acarretar os mais diversos problemas de saúde ligados a materiais radioativos (como tumores e cânceres). Mas, como a exposição a esse elemento é tão restrita, os casos de contaminação são nulos.
Referências:
https://web.archive.org/web/20191202132301/http://nautilus.fis.uc.pt:80/st2.5/scenes-p/elem/e08700.html
http://www.webelements.com/webelements/elements/text/Fr/index.html
Texto originalmente publicado em https://www.infoescola.com/elementos-quimicos/francio/