A matéria está sempre sujeita a transformações, que podem ser químicas ou físicas. As transformações químicas alteram a natureza dos compostos reagentes, gerando novas substâncias como produtos, como por exemplo, a queima (ou combustão) de papel. Já as transformações físicas são aquelas que não alteram a natureza do composto e não geram novas substâncias, como por exemplo, o ato de amassar um papel, ou o derretimento das calotas polares. Neste último caso, o que ocorre é uma transformação física chamada mudança de estado físico.
Toda matéria encontra-se em algum estado físico e, dependendo das condições de pressão e temperatura, pode passar para outros estados. Esse tipo de transformação está ocorrendo a todo tempo ao nosso redor, como, por exemplo, no gelo do nosso copo de suco, que está passando do estado sólido ao líquido, diluindo o suco e tornando-o mais “aguado”, ou ainda, no vapor que está presente no ar, que, ao entrar em contato com a superfície gelada do copo, vira líquido, formando gotas de água ao redor do copo gelado, dando a impressão do copo “suando”.
A passagem do estado sólido ao estado líquido é chamada de fusão, ou, como popularmente é conhecida, derretimento. O gelo, tanto das calotas polares, quanto do nosso copo de suco, se tornando água líquida é um exemplo de fusão. Outros exemplos que podem ser citados é o derretimento de uma vela acesa (fusão da parafina), o início do processo de fundição, em que se aquece um metal sólido até que se torne líquido, afim de torná-lo moldável, dentre outros.
Para que uma substância que se encontra em seu estado sólido passe para o líquido, é necessário fornecer energia para suas partículas. A energia fornecida será convertida em energia cinética, que causará maior agitação entre as partículas e, consequentemente, maior distanciamento entre elas, caracterizando o estado líquido, em que as forças de atração não são tão fortes como no estado sólido.
Sendo assim, podemos dizer que a fusão é um processo endotérmico, isto é, que absorve energia e, portanto, ocorre quando há um aumento da temperatura. Cada substância possui seu ponto de fusão, ou temperatura sob determinada pressão, na qual ela passa do estado sólido ao líquido. Em substâncias puras, trata-se de uma certa temperatura, que se mantém constante durante toda a transformação, já em misturas, a mudança ocorrerá numa determinada faixa, ou intervalo, de temperaturas, e em ambas, a pressão é mantida constante.
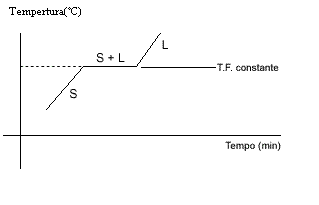
Gráfico mostra que a temperatura se mantém estável durante a fusão de uma substância pura.
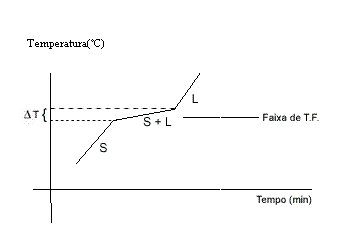
Gráfico mostra que a temperatura se altera durante a fusão de uma mistura.
Misturas eutéticas, entretanto, mesmo sendo misturas, possuem um comportamento diferente. As misturas eutéticas são formadas por determinadas substâncias, em proporções específicas, que tornam a fusão da mistura semelhante às de substâncias puras: sob temperatura determinada e constante.
Quando há variação na pressão, a temperatura de fusão sofrerá alteração. Caso a substância, em seu estado sólido, possua volume menor que em seu estado líquido (como a grande maioria dos compostos), isto é, quando se funde, há um aumento de volume, ao se aumentar a pressão, aumenta-se também a temperatura de fusão, pois terá seu processo dificultado, o que exigirá maiores temperaturas para ocorrer. Caso seja o contrário, em que a substância diminua de volume ao se fundir (como a água, o ferro, o antimônio, o bismuto), um aumento da pressão diminuirá a temperatura de fusão.
Texto originalmente publicado em https://www.infoescola.com/fisico-quimica/fusao/