A benzina possui sinônimos como nafta de petróleo, ligroína e éter de petróleo. A palavra éter é empregada para indicar volatilidade e não a presença de oxigênio. É uma mistura de solventes orgânicos, apolar, altamente inflamável, incolor, volátil e com odor semelhante a gasolina.
É obtido através da destilação do petróleo na faixa de temperatura de 35 - 90°C. Na sua composição predominam hidrocarbonetos alifáticos de cadeia C5 – C6, como o pentano e o hexano. Os hidrocarbonetos alifáticos podem ser divididos em vários grupos de acordo com o tipo da cadeia (aberta ou fechada) e o tipo de ligação entre os carbonos (simples, dupla ou tripla).
Por ser uma mistura de vários solventes suas características podem se diferenciar de acordo com a sua produção, promovendo algumas variações nas suas propriedades físico-químicas, que dever ser especificadas pelo fabricante. Na tabela abaixo encontram-se algumas propriedades físico-químicas gerais referentes à benzina.
| Propriedades físico-químicas | |
| Ponto de Ebulição | 35 a 60 ºC |
| Ponto de Fusão | < - 73 ºC |
| Ponto de Fulgor (vaso fechado) | - 57 ºC a -18 ºC |
| Solubilidade em água, 20ºC | 0,04% |
| Temperatura de auto-ignição | 232 a 290 ºC |
Fonte: http://cloud.cnpgc.embrapa.br/wp-content/igu/fispq/laboratorios/%C3%89ter%20de%20petr%C3%B3leo.pdf
Não se deve confundir benzina com benzeno. O benzeno é um hidrocarboneto aromático de fórmula molécula C6H6, composto apenas por um anel benzênico. A aromaticidade do anel confere características diferentes ao composto, como por exemplo, a realização de ressonância. Nas figuras abaixo estão representadas as estruturas do pentano, heptano e benzeno.
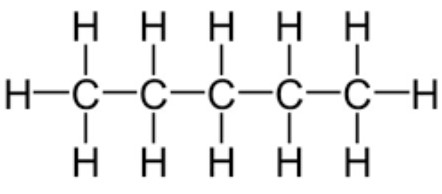
Pentano.
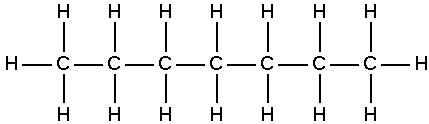
Heptano.
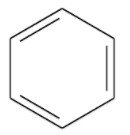
Benzeno.
O solvente orgânico é muito utilizado nas indústrias e laboratórios químicos farmacêuticos. Pode ser utilizado na composição de tintas, desengraxantes, removedores de adesivos, lavagem a seco, limpeza de metais, solvente extrator, entre outros. É muito utilizada na área da saúde, principalmente em hospitais para a retirada de curativos. Por ser um solvente lipossolúvel é absorvido facilmente pela pele e devido à sua toxicidade seu uso deve ser limitado.
É um solvente tóxico que quando inalado pode causar vômitos, dor de cabeça, tontura e em altas doses pode provocar convulsão ou até a morte. Contudo, a benzina é inalada para fins recreativos. É empregada na composição do lança-perfume, uma droga ilícita, potencializando os seus efeitos.
A benzina atinge o sistema nervoso central, assim ocasionando sentimentos solitários. Outros efeitos podem ser observados como prejuízos na memória e aprendizagem, metabólicos e funções nervosas. Durante a Segunda Guerra Mundial (1939 - 1945), foi frequentemente aplicada em injeções com o objetivo de assassinar pessoas nos campos de concentração.
Devido à preocupação com substâncias que agridem o meio ambiente, algumas empresas buscam soluções para a substituição de solventes tóxicos, e com isso, minimizar os riscos ambientais. Atualmente, existem vários produtos no mercado com baixa toxicidade que podem substituir a benzina em desengraxantes e agentes de limpeza.
Fontes:
http://cloud.cnpgc.embrapa.br/wp-content/igu/fispq/laboratorios/%C3%89ter%20de%20petr%C3%B3leo.pdf
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4194944/
http://webbook.nist.gov/chemistry/name-ser/
https://sites.google.com/site/curiosidadescombustiveis/derivados-do-petroleo-1/benzina
Texto originalmente publicado em https://www.infoescola.com/quimica/benzina/