A cromatografia é uma técnica quantitativa, tem por finalidade geral duas utilizações, a de identificação de substâncias e de separação-purificação de misturas. Usando propriedades como solubilidade, tamanho e massa.
Para o processo de separação de misturas, a mistura passa por duas fases sendo uma estacionaria (fixa, sendo um material poroso como um filtro) e outra móvel ( como um liquido ou um gás, que ajuda na separação da mistura), sendo que os constituintes dessa misturas interagem com as fases através de forças intermoleculares e iônicas, fazendo a separação. A mistura pode ser separada em varias partes distinta ou ainda ser purificada eliminando-se as substancia indesejáveis.
Para a identificação usa-se a comparação dos resultados da análise com outros resultados previamente conhecidos, como por exemplo, usa-se tabela de gráficos conhecidos e através desta compara-se os resultados obtidos que também são em gráficos achando-se os que mais se assemelham assim descobrindo quais as substancias que pertence a mistura.
Existem várias classificações quanto à cromatografia, os quatro principais são:
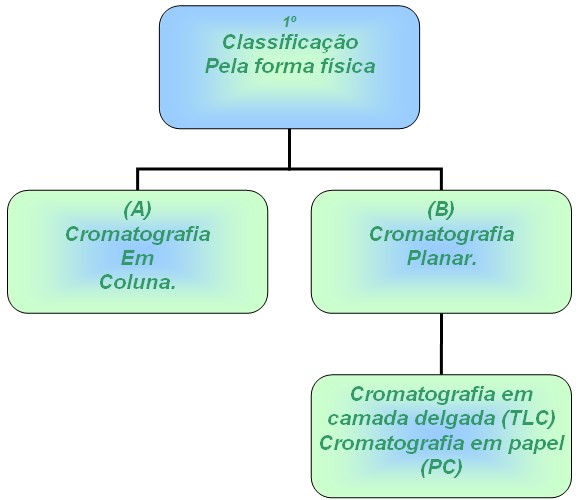
- Classificação pela forma física do sistema cromatográfico.
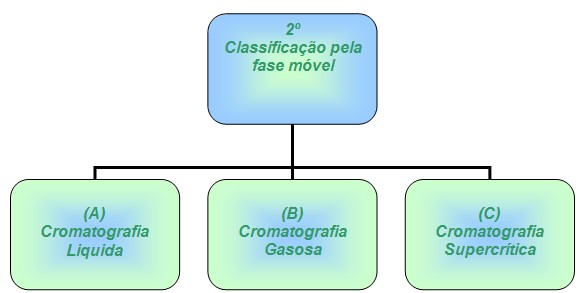
- Classificação pela fase móvel empregada.
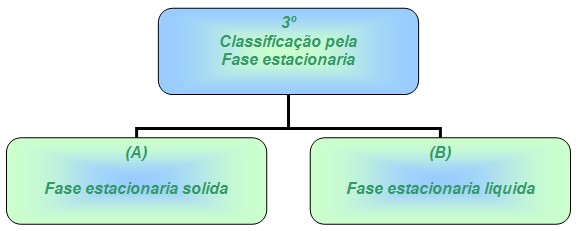
- Classificação pela fase estacionaria utilizada.
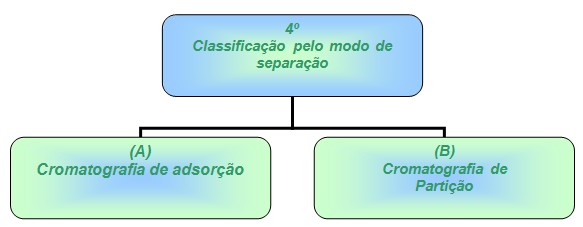
- Classificação pelo modo de separação.
(A) =  |
Nota-se que a mistura passa por duas fases ou filtros antes de se depositar no erlenmeyer. |
(B) = a fase estacionaria esta localizada sob uma placa PLANA ou em poros de papel, onde a fase móvel ou mistura atravessa através desses poros ou placa (CAMADA DELGADA).
(A) = a cromatografia liquida se dá quando a fase móvel é um liquido e a estacionaria é um solido, fazendo a separação através do sólido.
(B) = a cromatografia gasosa baseia-se quando a fase móvel é um gás e a estacionaria é um solido ou liquido.
(C) = a cromatografia supercrítica leva certas vantagens sobre aas outras duas, pode ser realizados analises não possíveis em cromatografia liquida ou gasosa.
(A) = Quando a fase fixa é um solido que serve como uma espécie de filtro, e age de varias maneiras para a separação da mistura
(B) = esta pode estar absorvida em um solido ou presa sobre ele, servindo com um filtro.
(A) = a cromatografia de adsorção é baseada em uma fase estacionaria solida que adsorve (prende) certas moléculas em seu meio, da parte móvel que deve ser liquida. Essa adsorção é devida a certas interações entre os constituintes da parte liquida e da solida.
(B) = a cromatografia de partição se dá pela diferença de solubilidade das substancias que devem ser liquidas, e sua separação se dá com o auxilio de filtros de papel ou em colunas como suporte.
Um exemplo de cromatografia de fácil entendimento é a cromatografia de tintas de canetas para descobrir qual a mistura de tintas usadas para a obtenção da cor especifica da caneta.
Parte estacionaria: papel filtro (filtro de café)
Parte móvel: álcool pode subir no filtro quando absorvido
Substancia (mistura): a tinta de caneta
O álcool avança sobre o papel filtro e à medida que sobe acaba desintegrando por forças moleculares as cores da tinta da caneta, demonstrando assim de quais cores ela é formada.
Referencias:
http://w3.ufsm.br/piquini/biomol09/cromatografia.ppt
https://web.archive.org/web/20061202163956/http://froque.no.sapo.pt:80/CROMATOGRAFIA-TLQ2.pdf
Texto originalmente publicado em https://www.infoescola.com/quimica/cromatografia/