O ácido cítrico ocorre nos frutos cítricos, como a laranja e, principalmente, o limão. Seu mais importante processo de obtenção se baseia na fermentação cítrica da glicose ou da sacarose (melaço) por meio de microorganismos como o Citromyces-Pfeferianus.
Entre os principais usos do ácido cítrico estão “alimentos e bebidas (64%), como aromatizante, detergentes e produtos de limpeza (22%), nos produtos farmacêuticos e nutricionais (10%), em produtos efervescentes, anticoagulantes e na Indústria cosmética (2%), para ajuste de pH e outras aplicações (2%)”1. O ácido cítrico é ainda utilizado como conservante e acidulante para determinados alimentos. “O ácido cítrico é um antioxidante usado como conservante natural, sendo conhecido também como acidulante IN 330. Proporciona sabor ácido e refrescante na preparação de alimentos e bebidas. Em bioquímica, é importante o seu papel como intermediário do ciclo do ácido cítrico, de forma que ocorre no metabolismo de quase todos os seres vivos. É ainda usado como produto de limpeza ecológico”2.
É o ácido orgânico mais usado na preparação de alimentos. É também empregado na indústria de bebidas efervescentes e de refrigerantes, na fabricação de confeitos e, como mordente em tinturaria; seu sal, o citrato de sódio, á laxativo.
Na molécula deste ácido, mostrada abaixo, estão presentes três grupamentos da função orgânica ácido carboxílico e um grupamento da função orgânica álcool. Dessa forma, trata-se de um ácido triprótico, ou seja, em meio aquoso, ioniza-se, liberando três mols de íons hidrogênio (H+) por cada mol de molécula. Dessa forma, a proporção de reação com o hidróxido de sódio (NaOH) é de um mol do ácido para três mols da base.
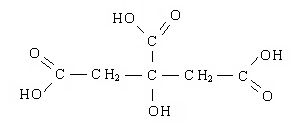
O experimento descrito abaixo visa a determinação da massa deste ácido presente em determinados frutos cítricos. Para tanto, pouca instrumentação é suficiente, e apenas serão necessários a solução padrão de NaOH e o indicador fenolftaleína. Com relação à solução padrão, deve estar na concentração de 1 molar, já o indicador na concentração de 1%.
PROCEDIMENTO EXPERIMENTAL
1. Pipetar para um erlenmeyer, 5,0 mL de suco de fruto cítrico previamente filtrado e diluir com alguns mililitros de água destilada. Preparar assim mais duas alíquotas.
2. Juntar duas gotas de solução alcoólica de fenolftaleína a 1,0 % a cada erlenmeyer.
3. Carregar a bureta com solução0,1 M de NaOH.
4. Gotejar a solução de hidróxido contida na bureta sobre o suco contido num dos erlenmeyers.
5. O aparecimento da coloração rosada no líquido contido no erlenmeyer indica o ponto final da titulação
Quando todo o ácido cítrico tiver sido neutralizado, uma primeira gota de solução de hidróxido de sódio em excesso conferirá ao meio de reação alcalinidade, e mudança na coloração do indicador de incolor (meio ácido) para róseo (meio básico), o que indica o referido ponto final.
6. Ler na bureta o volume gasto de solução dosadora.
7. Titular as outras alíquotas (preparadas conforme os itens 1 e 2).
8. Calcular o gasto médio de solução dosadora.
Referências:
1. http://www.eq.ufrj.br/biose/nukleo/aulas/Microbiol/eqb353_aula_17.pdf
2. http://www.conservantesliquidos.com.br/produtos/antioxidantes/acido-citrico-antioxidante.htm
PERUZZO, Francisco Miragaia (Tito); CANTO, Eduardo Leite; Química na Abordagem do Cotidiano, Ed. Moderna, vol.1, São Paulo/SP- 1998.
Texto originalmente publicado em https://www.infoescola.com/quimica/dosagem-de-acido-citrico-em-sucos-de-frutos-citricos/