A isomeria geométrica, também conhecida como isomeria cis-trans, é um tipo de estereoisomeria que engloba alcenos e moléculas cíclicas saturadas. Este é um tipo de isomeria espacial que, diferentemente da isomeria plana, os isômeros não são diferenciados pela sua fórmula estrutural plana, mas sim pela sua disposição no espaço. Assim, precisamos de modelos moleculares espaciais para conseguir identificar a isomeria.
Para compreendermos este tipo de isomeria devemos saber como funciona a divisão da molécula no plano. Devemos considerar uma linha imaginária no sentido vertical na molécula abaixo:
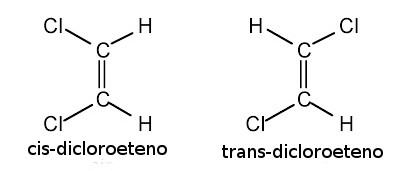
Condições para haver isomeria geométrica:
- Presença de dupla ligação onde é estabelecido o plano para rotação da molécula; ou ainda o composto ser cíclico e neste caso o próprio ciclo atua como a dupla ligação.
- Cada carbono da dupla apresentar ligantes diferentes.
Para desenharmos um isômero geométrico basta a molécula seguir os requisitos acima e então giramos um lado da molécula de forma que os grupamentos mudem de plano. Quando os grupamentos iguais estão para o mesmo lado do plano temos um isômero cis e quando estão para lados opostos temos o isômero trans.
Na figura das moléculas acima temos no primeiro caso um isômero cis, pois os dois átomos de hidrogênio estão localizados no mesmo lado do plano. Já na figura da direita os átomos de hidrogênio encontram-se transversais um ao outro.
São exemplos de aplicações da isomeria geométrica no cotidiano as gorduras presentes nos alimentos. Muito ouvimos falar atualmente nas gorduras trans, pois estas moléculas possuem este tipo de isomeria. Sabemos que este tipo de gordura é extremamente prejudicial ao nosso organismo podendo ocasionar aumento no colesterol, obstruções coronarianas e levar a sérios problemas cardíacos. Ela não é muito comum na natureza, porém é produzida para uso em alimentos industrializados a partir da gordura vegetal. Grandes quantidades desta gordura são encontradas em alimentos como bolos, bolachas recheadas e derivados. Já em menor quantidade encontramos na carne e no leite.
Os isômeros cis e trans tem propriedades físicas como ponto de fusão e de ebulição diferentes devido a diferença nas estruturas. As moléculas trans geralmente são mais estáveis que seus isômeros cis devido ao afastamento entre os grupamentos iguais que tendem a se repelir mais fortemente.
Quando a isomeria geométrica ocorre nos ciclos como no caso dos isômeros cis-1,2-dicloro-ciclopropano e trans – 1,2-dicloro-ciclopropano que aparecem na figura abaixo para identificarmos qual dos isômeros está representado devemos ver se os substituintes estão acima ou abaixo do núcleo, ou anel da molécula. Veja a seguir:
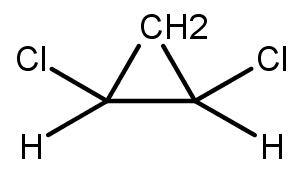
cis-1,2-dicloro-ciclopropano
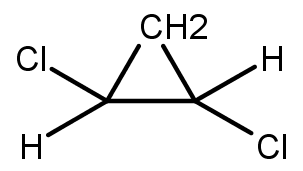
trans-1,2-diclorociclopropano
Neste caso podemos notar que no isômero Cis os grupamentos iguais, tanto átomos de hidrogênio quanto átomos de cloro estão para o mesmo lado do plano. Os átomos de cloro para cima e os de hidrogênio para baixo. E na segunda figura os grupamentos iguais estão para lados opostos do plano. Ou seja funciona basicamente como um alceno.
Notação E/Z
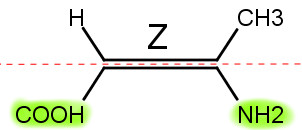
Para haver a notação E/Z a cadeia deve apresentar dois carbonos com pelo menos três ligantes diferentes entre si e neste caso a nomenclatura cis/trans seria insuficiente. Para esta notação devemos analisar os números atômicos dos átomos envolvidos. Quando os átomos de maior número atômico estiverem para o mesmo “lado” utilizamos a nomenclatura E (Entgegen que siginifica “opostos” em alemão) e se estiverem para lados opostos utilizamos a nomenclatura Z (Zusammen que significa “juntos” em alemão). Como no caso da figura abaixo:
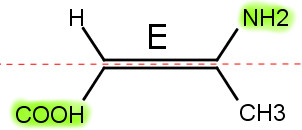
Texto originalmente publicado em https://www.infoescola.com/quimica/isomeria-geometrica/