Este é um tipo de isomeria espacial, ou seja, onde os isômeros são identificados pela sua disposição espacial. Tanto a isomeria óptica quanto a geométrica são exemplos de isomeria espacial.
O estudo da isomeria óptica é de extrema importância principalmente para a indústria farmacêutica, pois a eficácia de certos medicamentos e princípios ativos para certa doença pode ser determinada pela disposição espacial da molécula. Um caso de erro por falta de conhecimento de isomeria foi o da Talidomida que causou inúmeras deformidades em bebês de mulheres que ingeriam medicamento para ansiedade e que acabavam tendo efeito na formação fetal por ser utilizado o isômero do composto.
O requisito básico para um composto possuir isômero óptico é possuir ao menos um carbono quiral conferindo assimetria à molécula. Mas primeiramente, devemos definir o que é um carbono quiral.
O carbono é um elemento tetravalente, ou seja, precisa realizar quatro ligações para se estabilizar. Quando os quatro ligantes do carbono forem diferentes entre si dizemos que este é um carbono quiral ou assimétrico. Um composto quiral é opticamente ativo e um composto aquiral é inativo opticamente.
Por exemplo os compostos abaixo:
Nas figuras acima ambas estruturas possuem carbonos quirais, ou seja, que realizam ligação com quatro ligantes diferentes e neste caso são isômeras entre si pois somente mudam as posições espaciais dos átomos entre um e outro composto (observe a ordem dos átomos H, F e Br). Portanto ambas moléculas são assimétricas.
Um composto assimétrico pode ser classificado em dextrógiro ou levógiro e isso é definido a partir da incidência de um feixe de luz sobre a molécula. Se esse feixe for desviado para a direita temos um isômero dextrógiro e se for desviado para a esquerda temos um isômero levógiro. Caso o feixe de luz não seja desviado temos a presença de uma mistura racêmica. Uma mistura racêmica, ou racemato é resultado da proporção 1:1 de isômero dextrógiro e levógiro que acaba fazendo com que a mistura seja opticamente inativa.
Para quantificar esses isômeros utilizamos algumas fórmulas como por exemplo, para definir o número de isômeros ópticos de determinada molécula:
2n= número de isômeros ópticos
Onde: n= número de carbonos quirais presentes na molécula
Um enantiomorfo ou enantiômero é a imagem especular da molécula, funciona como se a mesma fosse projetada em um espelho plano conforme a figura abaixo:
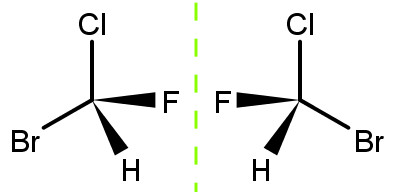
Neste caso faz-se analogia às mãos que são enantiomorfas, ou seja, são iguais quanto à estrutura, mas não podem ser sobrepostas.
Na isomeria óptica temos a nomenclatura R/S que indica o sentido do “giro” da molécula. Para definirmos isso precisamos:
- Ordenar os substituintes de acordo com a ordem de prioridade, e isso vai de acordo com o número atômico. Quanto maior o número atômico maior a prioridade. Ou seja, o hidrogênio quando aparecer será sempre o de menor prioridade.
- Posicionar a molécula de modo que o grupamento ou substituinte de menor prioridade fique “para trás”.
- Numerar os grupos da maior prioridade para a menor prioridade e ligar a sequência numérica; se a sequência ficar no sentido horário temos uma molécula R e se for anti-horário S.
Texto originalmente publicado em https://www.infoescola.com/quimica/isomeria-optica/