Os fenóis constituem uma das mais importantes funções da Química Orgânica. São compostos que possuem um ou mais grupamentos – OH (hidroxilas) ligados ao anel benzênico. Possuem fórmula geral Ar – OH e são encontrados no alcatrão da hulha e da madeira.
São utilizados como desinfetantes e germicidas, na conservação da madeira, na produção de explosivos, perfumes, na fabricação de reveladores fotográficos e antioxidantes.
Geralmente os fenóis são sólidos cristalinos. Quando puros são incolores. Podem apresentar coloração rósea porque oxidam-se facilmente. Possuem odor forte característico.
Possuem pontos de fusão e de ebulição superiores a de compostos de massa molecular semelhante, sem o grupo hidroxila, devido às ligações intermoleculares por pontes de hidrogênio. É mostrado na tabela abaixo algumas diferenças entre os pontos de mudança de fase do benzeno e do fenol.
| Nome | Fórmula | P.F. (0°C) | P.E. (0°C) | Ligações intermoleculares |
| benzeno | C6H6 | 5,5 | 80 | forças de Van der Waals |
| fenol | C6H5OH | 41 | 182 | pontes de hidrogênio |
Os compostos fenólicos são tóxicos, destroem todos os tipos de células. Devido a esta ação sobre os microorganismos, possuem ação anti-séptica e são usados como desinfetantes.
O fenol comum é também chamado hidroxibenzeno ou ácido fênico. Apresenta-se sob a forma de cristais e possui odor característico. É higroscópico e pouco solúvel em água (seu grau de solubilidade é de 9,3g por 100mL de água a25°C), apesar de ser o fenol mais hidrossolúvel. É solúvel em solventes orgânicos e soluções alcalinas. Em contato com a pele, produz manchas brancas, sendo que um contato mais prolongado possibilita sua penetração nos tecidos mais profundos, provocando queimaduras (ação cáustica).
É utilizado na fabricação do ácido pícrico, corantes sintéticos, fenolftaleína e baquelite. É ainda intermediário de diversas sínteses, e utilizado como corante.
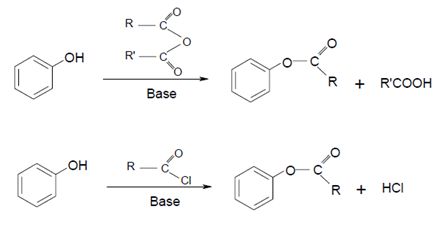
Entre algumas reações características dos fenóis, está a reação com anidridos de ácidos orgânicos, com formação de ésteres, cujo mecanismo pode ser observado na Figura 1. Nesta, pode ser visto que a reação com anidrido produz como subproduto, ao lado do éster, um ácido orgânico, ao passo que a reação direta entre éter e ácido carboxílico produz ácido inorgânico como subproduto.
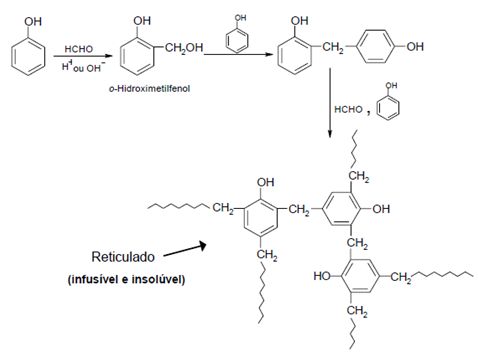
“O fenol pode reagir com o formaldeído para formar as reinas fenol-formaldeído, um dos polímeros sintéticos mais antigos (baquelite e novolac)”1. O mecanismo dessa reação pode ser observado na Figura 2, onde percebe-se o fenol como reagente de partida, bem como a sua participação, uma vez mais, como intermediário de reação.
Referências:
1. http://www.unirio.br/laqam/organica/aula_7.pdf
SARDELLA, Antônio; MATEUS, Edegar; Curso de Química: química geral, Ed. Ática, São Paulo/SP – 1995.
MAHAN, Bruce M.; MYERS, Rollie J.; Química: um curso universitário, Ed. Edgard Blucher LTDA, São Paulo/SP – 2002.
Texto originalmente publicado em https://www.infoescola.com/quimica/mecanismos-de-reacoes-dos-fenois/