Os metais pesados chumbo, prata e mercúrio apresentam efeito acumulativo no organismo, o que significa que a contaminação a partir dos mesmos acarreta em um acúmulo destes, de modo que o organismo não é capaz de expulsá-los naturalmente. Tais elementos encontram-se em pilhas, determinadas lâmpadas e algumas estruturas elétricas, requerendo cuidados em seu manuseio.
Este texto apresenta uma rota laboratorial para identificação e separação destes metais, a partir de seus íons em solução, de modo qualitativo (o que demonstra a não utilização de cálculos ou procedimentos quantificatórios).
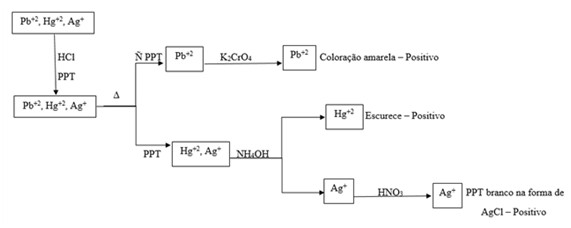
O Esquema 1 estabelece uma rota esquemática capaz de separar e identificar os íons Pb2+, Ag+ e Hg2+.
Esquema 1. Rota de identificação e de separação dos íons Pb2+, Ag+ e Hg2+.
Nesse esquema, pode-se observar que inicialmente os íons metálicos estão em uma mesma solução, a qual pode ser confirmada em relação à presença de cada um deles por uma reação com uma solução de ácido clorídrico (HCl), a partir de uma precipitação como teste positivo. Dessa forma, pode-se estabelecer a presença de pelo menos um desses íons na solução original.
Ao se aquecer esta solução, pode-se separar o íon chumbo, o qual é solúvel em altas temperaturas, podendo ser identificado pela coloração amarela da solução quando em reação com o dicromato de potássio (K2CrO7).
Após o aquecimento da solução original, poderão estar presentes no precipitado os íons mercúrio e chumbo. Ao se tratar a solução com hidróxido de amônio (NH4OH), pode-se identificar a presença de mercúrio a partir de um escurecimento da solução. Já ao se tratar a solução original com ácido nítrico (HNO3), a formação de um precipitado branco identifica a presença do íon prata.
Laboratorialmente, o descrito acima pode ser realizado por meio das seguintes etapas:
- Emprega-se 15 gotas da solução original e dilui-se com 10 mL de água;
- Adiciona-se HCl 3M até precipitação dos íons;
- Filtra-se;
- Rompe-se o papel filtro e com água transfere-se o precipitado para outro béquer;
- Ferve-se a solução por alguns minutos;
- Filtra-se imediatamente;
- Trata-se o filtrado com dicromato de potássio, onde observa-se uma coloração amarela; resultado positivo para chumbo;
- Trata-se diretamente o papel filtro com hidróxido de amônio, onde uma coloração negra mostra-se positiva na identificação do mercúrio;
- Recolhe-se o filtrado e adiciona-se algumas gotas de ácido nítrico concentrado ao mesmo, onde um precipitado branco mostra um resultado positivo para a prata, na forma de cloreto de prata.
Percebe-se, portanto, a possibilidade de separação e/ou identificação de cátions de uma amostra desconhecida (nas industrias são chamados efluentes), o que é possível utilizando-se técnicas e/ou procedimentos-padrões. Neste experimento, recebe-se uma amostra contaminada com metais pesados (Pb+2, Ag+ e Hg+2) e, por meio de reações específicas, pode-se separá-los e identificá-los.
Referências:
FELTRE, Ricardo, Química Orgânica, Ed. Moderna, 6ª Edição, São Paulo, 2004.
PERUZZO, Francisco; CANTO, Eduardo Leite, Química na abordagem do Cotidiano, Ed. Moderna, 3ª Edição, São Paulo, 2003.
Texto originalmente publicado em https://www.infoescola.com/quimica/rota-de-identificacao-e-separacao-para-os-ions-de-chumbo-prata-e-mercurio/